



3月12日,Cancer Cell 杂志在线发表题为 “Tumor repopulating cells induce PD-1 expression in CD8+ T cells by transferring kynurenine and AhR activation”的论文,基础医学研究所刘玉英副研究员和两名博士生梁晓雨、董文茜为本文的并列第一作者,黄波教授为通讯作者。
肿瘤免疫治疗是通过利用免疫细胞、免疫分子直接或间接杀伤肿瘤细胞,以产生控制或清除肿瘤的效果,被认为是人类战胜癌症的希望之所在,是当前肿瘤研究最热的领域。肿瘤免疫治疗主要依赖活化的T细胞对肿瘤细胞的杀伤,抑制性免疫分子(免疫检查点/checkpoint)PD-1在肿瘤组织中的T细胞表面上调表达,通过传递抑制信号阻止T细胞活化。目前针对免疫检查点PD-1的治疗性抗体已在临床肿瘤患者中取得史无前例的巨大成功,然而,PD-1抗体药物价格昂贵,且副作用大。因此,寻找PD-1的小分子阻断剂成为当前肿瘤免疫治疗药物研发的核心方向,但困难在于肿瘤组织中的T细胞上调表达PD-1分子的机理一直是一个谜。
色氨酸作为一种必须氨基酸,其在体内不仅通过代谢生成5羟色胺和褪黑素等重要活性分子,而且能够通过吲哚胺-2,3-双加氧酶(IDO)催化产生犬尿酸(Kyn)直接激活胞浆转录因子芳香族碳氢化合物受体(AhR)。黄波教授团队先前研究发现,高成瘤性的肿瘤再生细胞(Tumor repopulating cells,TRC)在肿瘤组织中,其IDO-Kyn-AhR通路非常活跃,而T细胞释放的免疫因子IFN-γ则进一步激活此通路,而诱导TRC进入休眠(Nat Commun. 2017;8:15207);另外该团队还发现抗病毒的免疫因子IFN-β同样激活此通路,并更强地诱导TRC休眠(J Clin Invest. 2018;128:1057-1073)。该团队将活化的T细胞和肿瘤细胞一起共培养后发现,活化的T细胞不但杀不死TRCs,反而上调表达PD-1,提示TRCs调节T细胞表达PD-1。通过大量研究,该团队证实了这一结论,然而其机理却十分复杂。活化的T细胞在肿瘤部位与TRC相互作用时,T细胞释放的IFN-γ促进TRCs显著上调色氨酸转运蛋白以及IDO,使得色氨酸大量进入TRCs并代谢为Kyn;Kyn被TRCs释放到细胞外后,通过T细胞膜表面的Kyn转运子,又进入到T细胞内,从而激活T细胞的AhR, AhR入核后直接结合PD-1启动子,启动PD-1的表达(见附图)。该机理的阐释,不但在理论上加深我们对当前肿瘤免疫的认识,而且实践上有望发展新的肿瘤免疫治疗策略。
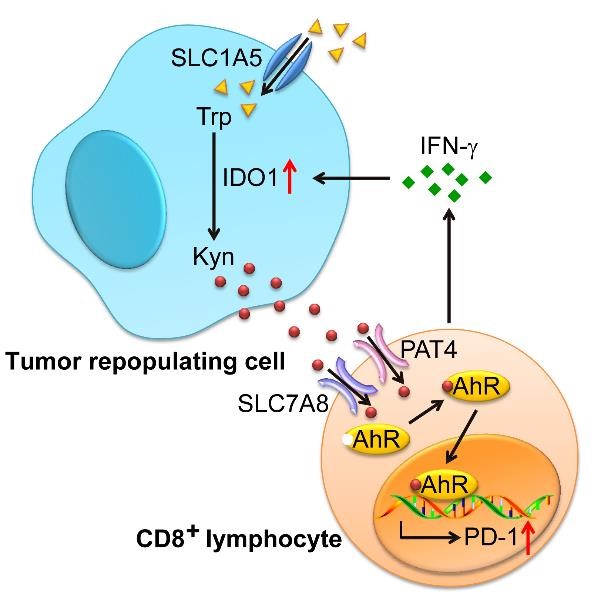
CD8+ T细胞上调表达PD-1
在免疫突触内,T细胞释放大量的IFN-γ,而IFN-γ一方面上调肿瘤细胞Trp转运子-SLC1A5表达,加大对Trp的摄取;另一方面上调IDO1表达,加快Trp代谢为Kyn。由此,大量Kyn释放到细胞外,通过T细胞表达的Kyn转运子,进入T细胞胞内,并激活T细胞的AhR, AhR入核结合PD-1启动子,启动PD-1表达。
3月16日,国际顶尖癌症研究期刊Cancer Discovery以Research Watch形式对此项研究进行了评述(The Kyn–AhR Pathway Upregulates PD-1 to Promote Tumor Immune Escape. Cancer Discov. March 16 2018 DOI:10.1158/2159-8290.CD-RW2018-048)。
该研究由黄波教授团队完成,并获得中国医学科学院医学与健康科技创新工程(2016-I2M-1-007)和国家自然科学基金的资助。基础医学研究所曹雪涛教授、药物研究所胡卓伟教授、苏州系统医学研究所秦晓峰教授参与了该项研究。