



来源 BioArt 2020年12月13日
肿瘤治疗的问题在于,极少的一小群具有干性的肿瘤细胞对当前各种治疗手段抵抗;而对于干性肿瘤细胞,其研究的困难又在于缺乏可靠的标志。目前,基于细胞表面分子如CD133或者酶如ALDH1等作为肿瘤干细胞研究手段时,非干性肿瘤细胞亦混杂其中。另外,这些化学分子不稳定,在不同肿瘤细胞类型中,变化非常大。这样,肿瘤干性难以界定的瓶颈,极大制约了对这类关键细胞更深入研究。
2020年12月4日,中国医学科学院&北京协和医学院免疫学系黄波团队在The EMBO Journal杂志上发表文章Cell softness regulates tumorigenicity and stemness of cancer cells,揭示了细胞物理的柔软性是干性肿瘤细胞内在的固有标志。这一研究工作将推动肿瘤干细胞研究领域的深入。

细胞作为自然的产物,不仅有化学的特征,同时还具备物理的特征。肌动蛋白actin聚合形成的微丝,是细胞骨架的基本组成,而肌球蛋白myosin则横跨并抓附于其上。肌球蛋白具有ATP酶活性,其水解ATP释放能量,转化为力,从而牵拉微丝,而这种力的牵拉,又使得细胞伸展并绷紧,从而具有了机械的硬度。细胞的机械力或者硬度采用压强(Pa,单位面积上所施加的力)来描述,可以通过原子力显微镜技术进行检测。
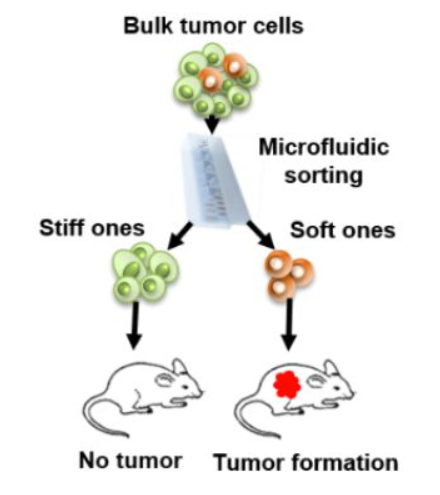
该研究发现,混合的肿瘤细胞群体中,绝大部分肿瘤细胞硬度大于0.7 KPa,而有数量非常少的肿瘤细胞,其硬度小于0.4 KPa。研究人员设计并制造微流控芯片仪器,能够对软的和硬的肿瘤细胞有效分选。他们发现,传统流式分选的CD133+、ALDH+或者侧群(SP)干性肿瘤细胞中,大部分肿瘤细胞硬度小于0.4 KPa,但也存在较大比例的硬的细胞,只有软的肿瘤细胞(100个)具有成瘤性,而硬的肿瘤细胞则不具备成瘤性。进一步基因组测序分析, Wnt信号调节蛋白BCL9L被鉴定出,其调控软的肿瘤细胞成瘤性和干性。
生物机械力是细胞本质性的特征之一,机械力生物学涉及细胞功能及生命活动的各个方面,是当今医学和生命科学最前沿研究领域和研究热点。运用生物机械力学原理和技术手段,有望在肿瘤学、免疫学、再生医学等诸多领域取得突破性、原创性的生物医学发现,为疾病诊治提供全新策略。该项研究的上述工作是对当前机械力生物学完美的诠释。
总之,这个研究工作的意义在于,揭示物理的机械软性是干性肿瘤细胞固有的内在标志,为干性肿瘤细胞深入研究提供技术支撑,并为临床靶向干性肿瘤细胞开辟新方向。同时,该项研究证实了体外培养的TRCs并非仅仅是人为培养的,其在肿瘤的瘤体内真实存在。
作为近几年崭露头角的新型交叉学科,开展机械力生物学研究的实验室很少。黄波课题组前期利用软的物理微环境,证明了干性肿瘤细胞能够在其间生长但不分化,从而建立体外扩增干性肿瘤细胞的方法,而该扩增的细胞被命名为肿瘤再生细胞(tumor-repopulating cell, TRC)(Nat Mater.2012;11(8):734-41)。与三维胶的软度相一致,TRCs具有很好的柔软性,易于变形。载药的肿瘤细胞来源的囊泡能够利用细胞的柔软性,从而更好地被TRCs摄取,而囊泡内的化疗药物则反过来将TRC杀伤(Cell Res. 2016;26(6):713-27)同时,载药囊泡能够被人为操作,变得更软,从而更好靶向化疗药物(Nat Biomed Eng.2020;4(7):743-753;Nat Biomed Eng.2019;3(9):729-740.)另外,黄波课题组还发现,TRCs在硬的基质中,能够进入休眠状态(Cancer Res.2018;78(14):3926-3937)。
相关论文信息:
https://www.embopress.org/doi/full/10.15252/embj.2020106123