



原创:生物谷 2021年3月27日
急性呼吸系统疾病综合征(ARDS)是COVID-19感染的主要临床症状。通常认为,失控的炎症与患者的死亡有关,并且针对关键的促炎细胞因子IL-6或JAK / STAT炎性途径的研究已经在8例重症COVID-19患者中进行了研究。压倒性的促炎细胞因子会损害肺泡上皮和内皮细胞,导致毛细血管通透性和肺纤维蛋白溶解,从而阻碍氧气(O2)和二氧化碳(CO2)的交换并导致缺氧,缺氧是引发COVID-19诱导死亡的关键因素。然而,低氧似乎出现在COVID-19的早期,而过度炎症则出现在相对晚期。临床实践已经观察到,许多COVID-19患者最初具有氧气剥夺而没有呼吸问题,这表明促炎性细胞因子之前的其他因素可能会导致COVID-19诱导的缺氧。
基于此,北京协和医学院免疫学系副主任黄波教授带领团队从8名COVID-19患者中收集了用于病理诊断的石蜡包埋的支气管肺泡灌洗液(BAL),通过HE染色、粘蛋白IHC染色、过碘酸-Schif试剂糖蛋白(PAS)染色等实验方法进行研究。研究结果以“Mucus production by IFN-AhR signaling triggers hypoxia of COVID-19 ”为题,在线发表在《Cell Research》杂志上。

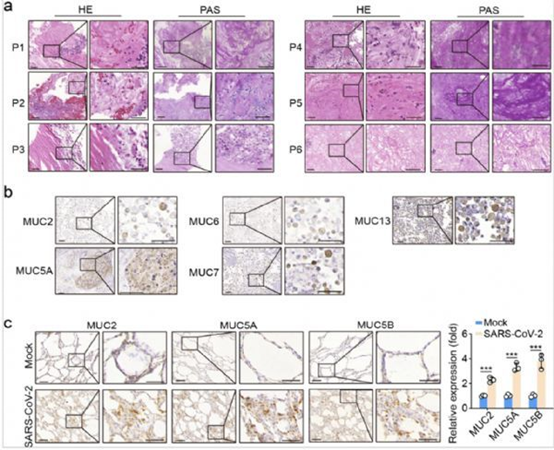
研究人员从8名COVID-19患者中收集了用于病理诊断的石蜡包埋的支气管肺泡灌洗液(BAL),发现粘液呈酸性(HE染色为红色),且富含碳水化合物(PAS阳性),并鉴定出一组粘蛋白(MUS),包括分泌的形成凝胶的粘蛋白2、5A,6和7以及与膜相连的粘蛋白13。同时发现在SARS-CoV-2感染的猕猴中,粘蛋白2、5A和5B的表达显著上调,这些结果表明粘液可能在COVID-19患者的肺上皮细胞中产生。
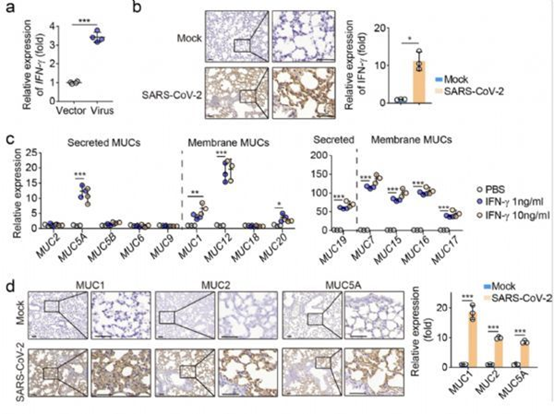
进一步研究发现,使用IFN-β或IFN-γ通过支气管雾化方法对小鼠进行治疗,发现IFN-β和IFN-γ能够降低SpO2,导致缺氧并同样增加Rrs(呼吸系统的阻力),Ers(呼吸系统的弹性),PV-k(压力/容积环的放气肢体上部曲率)和Eta(组织滞后性)。研究人员通过向小鼠静脉内注射AhR抑制剂来阻断AhR途径,消除了IFN-β-或IFN-γ引起的呼吸功能损害,尔后利用SARS-CoV-2感染了hACE2转基因小鼠,然后每天进行一次CH223191治疗,5天后粘蛋白1、4、5A,5B和16明显减少,并减少了肺部的病理损伤。这些结果表明AhR阻滞改善了SARS-CoV-2感染小鼠的肺部病理。
总之,在这项研究中,该研究团队表明粘蛋白在COVID-19患者的支气管肺泡灌洗液(BALF)中积累,并在严重呼吸综合征冠状病毒2(SARS-CoV-2)感染的小鼠和猕猴的肺中上调。 进一步研究发现,SARS-CoV-2感染后的IFN-β或IFN-γ可能会通过IDO-Kyn依赖性途径导致芳烃受体(AhR)活化,从而导致转录上调粘蛋白的表达,无论是分泌型还是分泌型。这些发现可能潜在地解释了COVID-19患者中“无声”缺氧的形成,表明通过靶向AhR途径可能恢复。
相关论文信息:
https://www.nature.com/articles/s41422-020-00435-z